
華東醫(yī)藥股份有限公司
-
中美華東醫(yī)藥品牌宣傳年度服務(wù)
策劃創(chuàng)意,原創(chuàng)插畫(huà),海報(bào)設(shè)計(jì),藥品包裝設(shè)計(jì)、折頁(yè)設(shè)計(jì)

中生復(fù)諾健生物科技(上海)有限公司
-
中國(guó)生物疫苗包裝設(shè)計(jì)
產(chǎn)品包裝設(shè)計(jì),材質(zhì)工藝建議

浙江金康醫(yī)藥有限公司
-
康恩貝制藥年度服,全案賦能,石特大健康與浙江金康醫(yī)藥年度合作碩果累累
醫(yī)藥品牌全案設(shè)計(jì)、藥品包裝升級(jí)、OTC產(chǎn)品手冊(cè)設(shè)計(jì)、中醫(yī)藥產(chǎn)品策劃、產(chǎn)品線形象整合、康恩貝集團(tuán)合作案例、醫(yī)藥營(yíng)銷物料設(shè)計(jì)、品牌視覺(jué)煥新

太極集團(tuán)四川綿陽(yáng)制藥有限公司
-
老藥新裝,價(jià)值重塑:石特大健康助力太極綿陽(yáng)制藥產(chǎn)品矩陣全面升級(jí)
醫(yī)藥包裝設(shè)計(jì),中成藥品牌升級(jí),OTC產(chǎn)品手冊(cè)設(shè)計(jì),藥品禮盒設(shè)計(jì),太極集團(tuán)包裝設(shè)計(jì),品牌全案設(shè)計(jì)

江蘇申命醫(yī)療科技有限公司
-
醫(yī)療器械全新產(chǎn)品策劃設(shè)計(jì)
包裝策劃,結(jié)構(gòu)設(shè)計(jì),包裝設(shè)計(jì),材質(zhì)工藝建議,打樣成品制作

人福普克藥業(yè)(武漢)有限公司
-
人福普克藥業(yè)出口系列包裝設(shè)計(jì)
系列規(guī)劃,系列產(chǎn)品設(shè)計(jì),印刷制作工藝建議

浙江華海藥業(yè)股份有限公司
-
華海藥業(yè)全系列包裝設(shè)計(jì)升級(jí)規(guī)范
品牌定位,產(chǎn)品規(guī)劃,包裝設(shè)計(jì)

浙江上藥九洲生物制藥有限公司
-
上海醫(yī)藥單品包裝設(shè)計(jì),仿制藥一致性評(píng)價(jià)
產(chǎn)品包裝設(shè)計(jì),復(fù)雜說(shuō)明書(shū)設(shè)計(jì),材質(zhì)工藝建議

浙江九洲生物醫(yī)藥有限公司
-
九洲藥業(yè)包裝系列化打造設(shè)計(jì)
系列策劃,包裝設(shè)計(jì),宣傳設(shè)計(jì)

江蘇福囍醫(yī)藥科技有限公司
-
品牌資產(chǎn)變現(xiàn):福囍醫(yī)藥多品類產(chǎn)品包裝的體系化落地設(shè)計(jì)
品牌包裝落地, 藥品系列化包裝, OTC產(chǎn)品包裝, 保健品包裝設(shè)計(jì), 品牌視覺(jué)應(yīng)用, 葫蘆符號(hào)設(shè)計(jì), 醫(yī)藥品牌全案設(shè)計(jì)公司
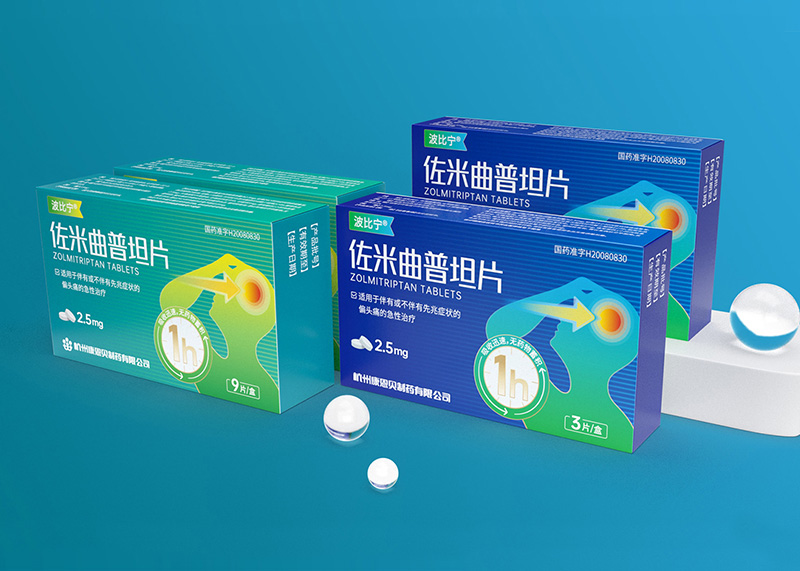
浙江金康醫(yī)藥有限公司
-
佐米曲普坦片藥品包裝升級(jí)設(shè)計(jì)
佐米曲普坦片藥品包裝設(shè)計(jì)

包頭東寶生物技術(shù)股份有限公司
-
東寶生物子品牌產(chǎn)品牛骨膠原肽粉包裝設(shè)計(jì)
品牌定位,產(chǎn)品規(guī)劃,包裝設(shè)計(jì)
【原創(chuàng)】百問(wèn)百答系列4期—— 一致性評(píng)價(jià)
mp.weixin.qq.com/s/bRdFHKv4GAfIzEEWLnGUIQ
01 社群精選問(wèn)答
問(wèn)題1:現(xiàn)在注射劑一致性評(píng)價(jià)在國(guó)家局網(wǎng)上申報(bào)系統(tǒng)里,是按補(bǔ)充申請(qǐng)還是一致性評(píng)價(jià)申請(qǐng)申報(bào)?
回答:一致性評(píng)價(jià)。
問(wèn)題2:一致性評(píng)價(jià)時(shí)申請(qǐng)BE實(shí)驗(yàn)時(shí)需要提交穩(wěn)定性資料嗎?處方工藝有變更和處方工藝無(wú)變更遞交資料時(shí)有什么不一樣嗎?
回答:一致性評(píng)價(jià)時(shí)申請(qǐng)BE實(shí)驗(yàn)時(shí),BE試驗(yàn)備案信息表里沒(méi)有要求提交穩(wěn)定性資料,仿制藥BE試驗(yàn)備案需要至少中試規(guī)模三批穩(wěn)定性數(shù)據(jù)(包括BE批),具體的可以看看備案信息表里的要求。三個(gè)月的穩(wěn)定性數(shù)據(jù)。處方工藝有變更和處方工藝無(wú)變更遞交資料時(shí),模塊一樣,具體內(nèi)容不一樣,無(wú)變更的填寫(xiě)原處方工藝,有變更的填寫(xiě)新的處方工藝。
問(wèn)題3:我們一致性評(píng)價(jià)品種,加速試驗(yàn)數(shù)據(jù)總雜大概是原研品種的2~3倍,但是在質(zhì)量標(biāo)準(zhǔn)范圍內(nèi),這種情況可以接受嗎?還是必須所有的數(shù)據(jù)都不劣于原研?
回答:在質(zhì)量標(biāo)準(zhǔn)范圍內(nèi),就叫質(zhì)量一致/不劣于。按質(zhì)量標(biāo)準(zhǔn)講,是可以接受的。但你們內(nèi)部得評(píng)估是否由于包材較原研差,導(dǎo)致的這種現(xiàn)象。還需要評(píng)估自制制劑和參比制劑加速試驗(yàn)時(shí)雜質(zhì)變化的趨勢(shì)是否相同,以考察二者穩(wěn)定性的差異。
問(wèn)題4:一致性評(píng)價(jià)時(shí),對(duì)一個(gè)產(chǎn)品,其標(biāo)準(zhǔn)已收載于藥典,但參比制劑為進(jìn)口產(chǎn)品,那一致性評(píng)價(jià)時(shí)的標(biāo)準(zhǔn)應(yīng)該參照哪個(gè)?藥典還是進(jìn)口標(biāo)準(zhǔn)?因?yàn)樗幍錁?biāo)準(zhǔn)通常會(huì)低于進(jìn)口標(biāo)準(zhǔn),尤其雜質(zhì)控制。
回答:仿制藥二條紅線:
——質(zhì)量標(biāo)準(zhǔn)高于或等于你能找到的任何標(biāo)準(zhǔn),尤其是法定標(biāo)準(zhǔn);
——實(shí)測(cè)數(shù)據(jù)高于或等于RLD;任何踩這兩條紅線的情況,都屬于重大風(fēng)險(xiǎn),需要十分慎重。藥典標(biāo)準(zhǔn)和進(jìn)口標(biāo)準(zhǔn),一條條對(duì)比,誰(shuí)高就用誰(shuí)。如果限度一樣但方法不同,還得證明誰(shuí)方法更好。
問(wèn)題5:國(guó)內(nèi)什么情況下“新注冊(cè)分類化藥仿制藥視同一致性評(píng)價(jià)”?
回答:六、按新注冊(cè)分類后批準(zhǔn)的仿制藥和新注冊(cè)分類申報(bào)批準(zhǔn)上市的仿制藥是否都視為通過(guò)一致性評(píng)價(jià)。答:根據(jù)總局2015年第230號(hào)文規(guī)定,新注冊(cè)分類實(shí)施后申報(bào)并批準(zhǔn)上市的仿制藥將是按與原研藥質(zhì)量和療效一致的原則進(jìn)行受理和審評(píng)審批。新注冊(cè)分類實(shí)施前受理并在實(shí)施后批準(zhǔn)的仿制藥,如企業(yè)選擇按原規(guī)定進(jìn)行審評(píng)審批,則需在藥品批準(zhǔn)上市3年內(nèi)需按照國(guó)發(fā)〔2015〕44號(hào)文件規(guī)定進(jìn)行質(zhì)量和療效一致性評(píng)價(jià)。仿制藥質(zhì)量和療效一致性評(píng)價(jià)工作政策問(wèn)答。
問(wèn)題6:一致性評(píng)價(jià)批準(zhǔn)后多久還可以用舊包裝?
回答:這個(gè)正常情況是立即執(zhí)行的,你這個(gè)需要跟地方省局申請(qǐng)也是可以,至于多久就看你溝通情況了。法規(guī)沒(méi)有明確規(guī)定時(shí)間,批件里面是照新批準(zhǔn)的說(shuō)明書(shū),標(biāo)準(zhǔn)和工藝執(zhí)行。一致性評(píng)價(jià)獲批后需要在國(guó)家局網(wǎng)上辦事大廳的業(yè)務(wù)系統(tǒng)中進(jìn)行備案,備案日期之后生產(chǎn)的產(chǎn)品 包裝按照備案執(zhí)行。但獲批到備案時(shí)間沒(méi)有明確規(guī)定。
問(wèn)題7:一致性評(píng)價(jià)可以沒(méi)有參比制劑嗎?
回答:有那種臨床價(jià)值明確但不推薦參比制劑的, 出了藥學(xué)研究指導(dǎo)意見(jiàn)那種可以沒(méi)有。基本都有的。名字就是質(zhì)量和療效一致性評(píng)價(jià),沒(méi)參比就沒(méi)標(biāo)桿,沒(méi)法評(píng)價(jià)。
問(wèn)題8:國(guó)家尚未推薦參比的口固制劑,可否進(jìn)行一致性評(píng)價(jià)?可用注射劑作為參比做一致性評(píng)價(jià)嗎?
回答:基于風(fēng)險(xiǎn),先進(jìn)行參比備案,國(guó)家批準(zhǔn)了再進(jìn)行一致性,不可以用注射劑做參比制劑。
問(wèn)題9:一致性評(píng)價(jià)中,原研產(chǎn)品需要一并做穩(wěn)定性嗎?一般原研產(chǎn)品要幾批,檢測(cè)點(diǎn)可以跳檢嗎?
回答:質(zhì)量對(duì)比研究一般原研要3批,穩(wěn)定性原研一批即可。原研要按指導(dǎo)原則來(lái),穩(wěn)定的品種是不需要的,一般都是放進(jìn)去對(duì)比一下第六個(gè)月雜質(zhì)譜,不穩(wěn)定的品種就需要了,重點(diǎn)在看趨勢(shì),可以看一下華海那個(gè)帶條件批準(zhǔn)的品種。
問(wèn)題10:一個(gè)品種未過(guò)一致性評(píng)價(jià),選擇增加規(guī)格,對(duì)增加規(guī)格的品種進(jìn)行一致性評(píng)價(jià),那增加規(guī)格和一致性評(píng)價(jià)可以同時(shí)申報(bào)嗎?
回答:按一致性研究,增的規(guī)格處方工藝與原規(guī)格不一樣,BE要重做。
問(wèn)題11:進(jìn)口仿制藥一致性評(píng)價(jià),不改變?cè)o料來(lái)源的,原輔料沒(méi)有登記,也無(wú)法在資料中提供登記資料,是否可以?
回答:可不登記,但必須按要求提供登記資料。參考以下公告:CFDA 總局關(guān)于調(diào)整原料藥、藥用輔料和藥包材審評(píng)審批事項(xiàng)的公告(2017年第146號(hào)) 290190715,國(guó)家藥監(jiān)局關(guān)于進(jìn)一步完善藥品關(guān)聯(lián)審評(píng)審批和監(jiān)管工作有關(guān)事宜的公告(2019年第56號(hào))
問(wèn)題12:一致性評(píng)價(jià)品種,原品種說(shuō)明書(shū)和原研的有出入,以哪個(gè)為準(zhǔn)來(lái)確定終稿說(shuō)明書(shū)呢?
回答:按照原研的。說(shuō)明書(shū)會(huì)有審評(píng)中心老師找你溝通的。若有一致性評(píng)價(jià)已經(jīng)過(guò)了的廠家,可以從CDE找到他們的說(shuō)明書(shū),跟他們一樣即可。根據(jù)以上原則,先交上去。
問(wèn)題13:我們公司要做一個(gè)注射劑一致性評(píng)價(jià),但同時(shí)想增加兩個(gè)規(guī)格,這怎么申報(bào)?沒(méi)有批文,就是增加原研或參比制劑已有的規(guī)格?
回答:一致性評(píng)價(jià)申請(qǐng)按品種管理,開(kāi)通新增藥品規(guī)格的補(bǔ)充申請(qǐng)直接申報(bào)一致性評(píng)價(jià)途徑。為了防止規(guī)格濫用,新增加的藥品規(guī)格需符合臨床合理用法用量范圍,且與原研(參比制劑)一致。
問(wèn)題14:一致性評(píng)價(jià)標(biāo)識(shí)印在標(biāo)簽小盒有什么尺寸限制或要求嗎?
回答:20170825總局關(guān)于仿制藥質(zhì)量和療效一致性評(píng)價(jià)工作有關(guān)事項(xiàng)的公告(2017年第100號(hào))。
問(wèn)題15:一致性評(píng)價(jià),顯示在藥審中心審評(píng)狀態(tài),目前進(jìn)度是完成生產(chǎn)和研發(fā)現(xiàn)場(chǎng)考核后并已經(jīng)完成第一次發(fā)補(bǔ)。想在審評(píng)中遞交變更上市持有人申請(qǐng),持有人從子公司變成母公司。這種情形是不是也適用于上市后變更管理辦法中的持有人變更管理?
回答:審評(píng)中可以對(duì)申請(qǐng)人名稱變更可以書(shū)面告知CDE,并提交相關(guān)證明性材料,審評(píng)中變更持有人應(yīng)該是不可以。獲批后變更持有人的路徑,就參考上市后變更管理辦法。
問(wèn)題16:《化學(xué)藥品注射劑仿制藥質(zhì)量和療效一致性評(píng)價(jià)技術(shù)要求》中要求“注射劑中輔料種類和用量通常應(yīng)與參比制劑(RLD)相同。輔料的用量相同是指仿制藥輔料用量為參比制劑相應(yīng)輔料用量的95%—105%”,那么注射劑一致性評(píng)價(jià)時(shí)需要將各輔料的含量檢測(cè)項(xiàng)定入最終的質(zhì)量標(biāo)準(zhǔn)中嗎?
回答1:這個(gè)跟輔料含量沒(méi)有關(guān)系,你處方比例一致就行了。應(yīng)該是處方中的加入量,在制劑的成品質(zhì)量標(biāo)準(zhǔn)中是不定入的。回答2 :參比制劑解析時(shí)可以測(cè)定各輔料含量,然后自制制劑處方研究時(shí)參考。
問(wèn)題17:按照新分類上報(bào)的制劑,批準(zhǔn)后,是否可視為已通過(guò)一致性評(píng)價(jià)?還是后續(xù)要做一致性評(píng)價(jià)的?
回答:視為通過(guò)一致性評(píng)價(jià)。六、按新注冊(cè)分類后批準(zhǔn)的仿制藥和新注冊(cè)分類申報(bào)批準(zhǔn)上市的仿制藥是否都視為通過(guò)一致性評(píng)價(jià)。答:根據(jù)總局2015年第230號(hào)文規(guī)定,新注冊(cè)分類實(shí)施后申報(bào)并批準(zhǔn)上市的仿制藥將是按與原研藥質(zhì)量和療效一致的原則進(jìn)行受理和審評(píng)審批。新注冊(cè)分類實(shí)施前受理并在實(shí)施后批準(zhǔn)的仿制藥,如企業(yè)選擇按原規(guī)定進(jìn)行審評(píng)審批,則需在藥品批準(zhǔn)上市3年內(nèi)需按照國(guó)發(fā)〔2015〕44號(hào)文件規(guī)定進(jìn)行質(zhì)量和療效一致性評(píng)價(jià)。《仿制藥質(zhì)量和療效一致性評(píng)價(jià)工作政策問(wèn)答》。
問(wèn)題18:注射劑需要做BE嗎?已上市化學(xué)仿制藥(注射劑)一致性評(píng)價(jià)技術(shù)要求(征求意見(jiàn)稿)是有提到需要做。
回答:一般注射劑免BE,對(duì)于特殊注射劑,需要做BE,與普通注射劑相比,特殊注射劑的質(zhì)量及其活性成分的體內(nèi)行為受處方和工藝的影響較大,可能進(jìn)一步影響制劑在體內(nèi)的安全性和有效性,首先開(kāi)展受試制劑與參比制劑藥學(xué)及非臨床的比較研究,然后進(jìn)行人體生物等效性研究,必要時(shí)開(kāi)展進(jìn)一步的臨床研究。對(duì)于FDA或EMA已公布指導(dǎo)原則的特定注射劑品種,建議參照FDA或EMA技術(shù)要求開(kāi)展與參比制劑的對(duì)比研究。
問(wèn)題19:一致性評(píng)價(jià)的申報(bào)資料還是按著2016年的120號(hào)文件對(duì)嗎?新注冊(cè)分類申報(bào)的,就是按M4格式要求提交?
回答:一致性評(píng)價(jià)品種按照120文提交申報(bào)資料,按補(bǔ)充申請(qǐng)?zhí)峤弧P伦?cè)分類的按照M4格式要求。
問(wèn)題20:一致性評(píng)價(jià)是不需要經(jīng)過(guò)NMPA最后批準(zhǔn),由CDE直接行政審批的是嗎?
回答:所有的補(bǔ)充申請(qǐng)都是CDE批準(zhǔn),不需要送注冊(cè)司發(fā)件,都是CDE直接發(fā)批件
問(wèn)題21:我們有個(gè)口服溶液劑已按照一致性評(píng)價(jià)的要求完成了相關(guān)研究工作,是否就是按照補(bǔ)充申請(qǐng)途徑申報(bào)呢?能拿到過(guò)評(píng)的批準(zhǔn)件嗎?
回答:現(xiàn)在一致性評(píng)價(jià)就口服固體制劑和注射劑,按照補(bǔ)充申請(qǐng)申報(bào)過(guò)評(píng)可以視同通過(guò)一致性。
問(wèn)題22:仿制藥申請(qǐng)視同一致性評(píng)價(jià),在哪個(gè)法規(guī)里面有規(guī)定啊?
回答:NMPA公告2017年第100號(hào)。
問(wèn)題23:一致性評(píng)價(jià)的時(shí)候可以把原輔包的供應(yīng)商一起變了嗎?
回答:可以。
問(wèn)題24:一致性評(píng)價(jià)雜質(zhì)部分是只寫(xiě)已知雜質(zhì)嗎?和原研雜質(zhì)比對(duì)是放這里嗎?
回答:全面的雜質(zhì)分析都需要寫(xiě)的,研究中發(fā)現(xiàn)的新的降解雜質(zhì),以及各國(guó)藥典中對(duì)API和制劑的雜質(zhì)要求及質(zhì)量對(duì)比都要有,寫(xiě)在8.5.5章節(jié)。
問(wèn)題25:按照一致性評(píng)價(jià)要求做滴眼液,原研防腐劑用量能夠查到,檢測(cè)也是0.03%,自制品和參比抑菌效力都沒(méi)通過(guò),因此將防腐劑用量篩選做完后選擇了0.06%。相當(dāng)于已經(jīng)超過(guò)了±5%的要求,CDE這邊雖然暫時(shí)沒(méi)有對(duì)眼科藥出臺(tái)具體的指導(dǎo)原則,但是按照《眼科仿制藥質(zhì)量和療效一致性評(píng)價(jià)的基本思路 》這篇文章來(lái)看,CDE暫時(shí)的思路還是參考FDA那邊的,所以變更了輔料的用量(也就是Q2不同),原則上是應(yīng)該做BE而不是安全性評(píng)價(jià)(刺激性實(shí)驗(yàn)屬于安全性評(píng)價(jià)的一部分內(nèi)容,本來(lái)在ANDA時(shí)就需要做的,能不能拿安評(píng)實(shí)驗(yàn)的一部分來(lái)代替BE?(這個(gè)可能不合理)如果不做BE,有沒(méi)有不批準(zhǔn)的風(fēng)險(xiǎn)?
回答:眼科的BE相當(dāng)于做個(gè)驗(yàn)證性臨床了,成本還是很高的。超過(guò)了Q2的要求,理論上市需要做BE的(溶液型滴眼液),如果不做BE,需要證明差異對(duì)安全性有效性無(wú)影響,這個(gè)就不好證明了,要結(jié)合適應(yīng)癥來(lái)分析。通常來(lái)說(shuō)原研產(chǎn)品的質(zhì)量可控性已經(jīng)經(jīng)過(guò)FDA的審核,沒(méi)有問(wèn)題的,抑菌效力不合格是不是方法有問(wèn)題,或者要求太嚴(yán)格了。給個(gè)建議,日本有用動(dòng)物來(lái)驗(yàn)證差異的,但是FDA沒(méi)見(jiàn)過(guò)這樣的操作,CDE不一定會(huì)認(rèn)可,如果是國(guó)內(nèi)首家上市,認(rèn)為這個(gè)差異可以接受,后續(xù)通過(guò)驗(yàn)證性臨床來(lái)證明安全性有效性。
問(wèn)題26:已過(guò)一致性評(píng)價(jià)的品種新增規(guī)格,是按照一致性評(píng)價(jià)申報(bào)還是直接按照重大變更的補(bǔ)充申請(qǐng)報(bào)?
回答:可以按照一致性評(píng)價(jià)申報(bào)。
問(wèn)題27:一致性評(píng)價(jià)申請(qǐng)是否可以關(guān)聯(lián)變更生產(chǎn)場(chǎng)地?有2個(gè)工廠,批文的生產(chǎn)地址在A工廠,一致性評(píng)價(jià)直接在B工廠進(jìn)行,是否可以?
回答:可以,甚至可以變更規(guī)格附帶申請(qǐng)一致性評(píng)價(jià)。這是兩個(gè)申請(qǐng)事項(xiàng)。一致性評(píng)價(jià)申請(qǐng)是國(guó)家局補(bǔ)充申請(qǐng)形式,根據(jù)生產(chǎn)監(jiān)督管理辦法變更生產(chǎn)場(chǎng)地屬于省局的監(jiān)管范疇。
問(wèn)題28:我公司現(xiàn)在僅有某品種10mg規(guī)格,請(qǐng)問(wèn)這時(shí)候可以做一個(gè)20mg規(guī)格申報(bào)一致性評(píng)價(jià),同時(shí)豁免10mg規(guī)格的品種,就是增加一個(gè)規(guī)格來(lái)申報(bào)一致性評(píng)價(jià)。是否可以這種操作?
回答:可以,能否豁免10mg,需要根據(jù)兩個(gè)規(guī)格的處方是否為等比例變化,而且體外溶出相似。

問(wèn)題29:我們有個(gè)注射劑品種大規(guī)格已經(jīng)通過(guò)一致性評(píng)價(jià)獲得批件后,增加規(guī)格按一致性評(píng)價(jià)通道走的,現(xiàn)在受理老師讓我們撤回按補(bǔ)充申請(qǐng)走,說(shuō)要同時(shí)申報(bào)才按一致性評(píng)價(jià)走,想知道有沒(méi)有和我一樣情況的?
回答:我們單獨(dú)申報(bào)后,可以按照一致性評(píng)價(jià)。
問(wèn)題30:一致性評(píng)價(jià)是做完驗(yàn)證三批,就可以直接上BE了是嗎?有穩(wěn)定性數(shù)據(jù)6個(gè)月就可以申報(bào)了對(duì)嗎?具體是哪個(gè)法規(guī)出來(lái)的?國(guó)家藥監(jiān)局藥審中心關(guān)于發(fā)布《化學(xué)藥品注射劑仿制藥質(zhì)量和療效一致性評(píng)價(jià)技術(shù)要求》等3個(gè)文件的通告(2020年第2號(hào))是這個(gè)嗎?
回答1:?BE備案表和一致性評(píng)價(jià)申報(bào)資料。回答2:?一致性評(píng)價(jià)產(chǎn)品是生產(chǎn)完就可以立即進(jìn)行be備案,3、4類產(chǎn)品,生產(chǎn)完后有三個(gè)月穩(wěn)定性數(shù)據(jù)才能去BE備案。
問(wèn)題31:新增加規(guī)格目前能不能按照4類仿制藥申報(bào)呢?或者按補(bǔ)充申請(qǐng)報(bào)的話目前會(huì)不會(huì)視為通過(guò)一致性評(píng)價(jià)呢?
回答1:

回答2:我們不久前剛提交了一個(gè)通過(guò)一致性評(píng)價(jià)通道增加規(guī)格的補(bǔ)充申請(qǐng),新增規(guī)格有參比制劑的話,受理是沒(méi)問(wèn)題的。我們是注射液,參照注射液那個(gè)一致性評(píng)價(jià)要求來(lái)的。
問(wèn)題32:我們的是滴眼劑,滴眼劑現(xiàn)在還沒(méi)有出來(lái)一致性評(píng)價(jià)的法規(guī),不知道這么操作行不行。
回答:可以先和CDE溝通,不過(guò)沒(méi)有法規(guī),你們這種申報(bào)會(huì)不會(huì)不受理。
問(wèn)題33:仿制藥一致性評(píng)價(jià)申報(bào)資料要求應(yīng)該繼續(xù)參照2016年80號(hào)文還是應(yīng)該參照新的《化學(xué)藥品注冊(cè)受理審查指南(試行)》(2020年第10號(hào))?
回答:仿制藥一致性評(píng)價(jià)申報(bào)資料要求應(yīng)該繼續(xù)參照2016年120號(hào)文。
問(wèn)題34:關(guān)于注射劑一致性評(píng)價(jià)的問(wèn)題. 注射劑一致性評(píng)價(jià)產(chǎn)品為了和參比制劑的處方用量一致,將其中一種輔料的用量微調(diào),其他不變,和參比制劑保持一致,這樣需要做非臨床研究么?比如局部耐受性的刺激性、耐受性、溶血性等。
回答:如果再評(píng)價(jià)產(chǎn)品的處方工藝均發(fā)生了變化,需要進(jìn)行開(kāi)展過(guò)敏性(局部、全身和光敏毒性)、溶血性和局部(血管、皮膚、粘膜、肌肉等)刺激性等特殊安全性試驗(yàn)。
問(wèn)題35:A膠囊一致性評(píng)價(jià)首家過(guò)評(píng)時(shí)間為2019年11月1日;A片一致性評(píng)價(jià)過(guò)評(píng)時(shí)間為2020年8月10日,A分散片一致性評(píng)價(jià)過(guò)評(píng)時(shí)間為2021年6月8日。我司產(chǎn)品為A分散片,要和哪個(gè)時(shí)間為起始的3年期限必須完成一致性評(píng)價(jià)?同一成分,劑型不同也屬于不同品種?
回答:應(yīng)該以2019年11月1日這個(gè)時(shí)間為起始的3年期限必須完成一致性評(píng)價(jià);2018.12.28《關(guān)于仿制藥質(zhì)量和療效一致性評(píng)價(jià)有關(guān)事項(xiàng)的公告》政策解讀八、仿制藥評(píng)價(jià)時(shí)限如何調(diào)整?
答:化學(xué)藥品新注冊(cè)分類實(shí)施前批準(zhǔn)上市的含基本藥物品種在內(nèi)的仿制藥,自首家品種通過(guò)一致性評(píng)價(jià)后,其他藥品生產(chǎn)企業(yè)的相同品種原則上應(yīng)在3年內(nèi)完成評(píng)價(jià)。考慮到藥品臨床需求存在地域性和時(shí)效性等特點(diǎn),為確保市場(chǎng)供應(yīng)和人民群眾用藥可及性,企業(yè)未能按上述要求完成評(píng)價(jià)的,經(jīng)評(píng)估認(rèn)為屬于臨床必需、市場(chǎng)短缺的品種,可向所在地省級(jí)藥監(jiān)部門(mén)提出延期評(píng)價(jià)申請(qǐng),說(shuō)明理由并提供評(píng)估報(bào)告,省級(jí)藥監(jiān)部門(mén)會(huì)同衛(wèi)生行政部門(mén)組織研究論證,經(jīng)研究認(rèn)定為臨床必需、市場(chǎng)短缺品種的,可適當(dāng)予以延期,原則上不超過(guò)5年。同時(shí),對(duì)同意延期的品種,省級(jí)藥監(jiān)部門(mén)會(huì)同相關(guān)部門(mén)要繼續(xù)指導(dǎo)、監(jiān)督并支持企業(yè)開(kāi)展評(píng)價(jià)工作。屆時(shí)仍未完成的,藥監(jiān)部門(mén)不予批準(zhǔn)其藥品再注冊(cè)申請(qǐng)。這里強(qiáng)調(diào)的是品種不是劑型。就像集采名單同一個(gè)品種下面有不同的劑型
問(wèn)題36:我們有一個(gè)進(jìn)口產(chǎn)品還沒(méi)有申報(bào)一致性評(píng)價(jià)的補(bǔ)充申請(qǐng),但是這個(gè)產(chǎn)品有一家已經(jīng)通過(guò)了一致性評(píng)價(jià)了。我們的注冊(cè)證馬上要到期了,現(xiàn)在要開(kāi)始報(bào),再注冊(cè)申請(qǐng)了,如果這樣的話,CDE能批這個(gè)再注冊(cè)的申請(qǐng)嗎?
回答:請(qǐng)參考 2018年12月28日發(fā)布的《關(guān)于仿制藥質(zhì)量和療效一致性評(píng)價(jià)有關(guān)事項(xiàng)的公告》政策解讀,化學(xué)藥品新注冊(cè)分類實(shí)施前批準(zhǔn)上市的含基本藥物品種在內(nèi)的仿制藥,自首家品種通過(guò)一致性評(píng)價(jià)后,其他藥品生產(chǎn)企業(yè)的相同品種原則上應(yīng)在3年內(nèi)完成評(píng)價(jià)。考慮到藥品臨床需求存在地域性和時(shí)效性等特點(diǎn),為確保市場(chǎng)供應(yīng)和人民群眾用藥可及性,企業(yè)未能按上述要求完成評(píng)價(jià)的,經(jīng)評(píng)估認(rèn)為屬于臨床必需、市場(chǎng)短缺的品種,可向所在地省級(jí)藥監(jiān)部門(mén)提出延期評(píng)價(jià)申請(qǐng),說(shuō)明理由并提供評(píng)估報(bào)告,省級(jí)藥監(jiān)部門(mén)會(huì)同衛(wèi)生行政部門(mén)組織研究論證,經(jīng)研究認(rèn)定為臨床必需、市場(chǎng)短缺品種的,可適當(dāng)予以延期,原則上不超過(guò)5年。同時(shí),對(duì)同意延期的品種,省級(jí)藥監(jiān)部門(mén)會(huì)同相關(guān)部門(mén)要繼續(xù)指導(dǎo)、監(jiān)督并支持企業(yè)開(kāi)展評(píng)價(jià)工作。屆時(shí)仍未完成的,藥監(jiān)部門(mén)不予批準(zhǔn)其藥品再注冊(cè)申請(qǐng)。
問(wèn)題37:新仿制藥,增加規(guī)格,通過(guò)審評(píng)后,可以直接視同通過(guò)一致性評(píng)價(jià)嗎?申請(qǐng)表和資料中需要特殊備注嗎?
回答:根據(jù)《藥品注冊(cè)管理辦法》及其相關(guān)規(guī)定,增加藥品規(guī)格為補(bǔ)充申請(qǐng)事項(xiàng)。增加規(guī)格,通過(guò)審評(píng)后,可以直接視同通過(guò)一致性評(píng)價(jià),可以參考華潤(rùn)賽科藥業(yè)有限責(zé)任公司左乙拉西坦片(0.25g)。

 0571-88685587
0571-88685587 15605889708
15605889708